JFE-TEC News
No.47「医薬品中元素不純物分析(ICH Q3D対応)」
JFE-TEC News No.47号 リチウムイオン二次電池の分析・評価技術(4) 他 記事一覧
医薬品中元素不純物分析(ICH Q3D対応)
全文 PDF (1.2 MB)
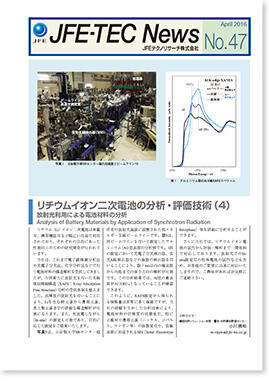
No.47 リチウムイオン二次電池の分析・評価技術(4) 他
医薬品中元素不純物分析(ICH Q3D対応)
Element Impurities Analysis of Pharmaceutical Products
医薬品中の元素不純物には、原薬を合成するために意図的に用いられた触媒の残留物や不可避的に混入する有害元素等があり、医薬品の安全性を確認するために、これらの含有量を許容限度値内に管理する必要があります。平成27年9月30日には「元素不純物ガイドラインQ3D:ICH 合意ガイドライン(薬食審査発0930第4号)」が発行され、平成29年4月1日以降に承認申請される新医薬品についてはガイドラインに基づき製剤中の対象元素不純物に十分なリスクアセスメントを行うように定められました。

写真 クリーンルーム内に設置したICP質量分析装置
当社ではこのようなニーズの拡大に対応するため、金属・半導体・有機材料など様々な分野の多様な分析で培った極微量元素分析技術を結集し、汚染の少ない最適な試料前処理で溶液化した製品、原薬、中間体等の様々な試料を高感度型ICP質量分析装置(写真)で分析するシステムを構築いたしました。PDE値(1日許容暴露量)との比較評価に十分なμg、ngレベルの分析値のご提供が可能です。
また医薬品の試験検査においては、厳格な品質管理システムが求められ、その内容は「医薬品及び医薬部外品の製造管理及び品質管理の基準に関する省令」(GMP省令)に定められています。当社ではGMP省令に基づいた試験検査の品質管理システムを整え、コンピューターシステム(LIMS)により品質管理を行うなど、他の受託分析機関には無い厳格な施設環境を整えています。
元素不純物のリスクアセスメントに先立って、元素不純物含有の有無をppmレベルまで定性的に評価する分析も承りますので、お気軽にご相談ください。
関連リンク・関連記事
このページに関する
お問い合わせはこちらから
- JFEテクノリサーチ株式会社 営業本部
- 0120-643-777


